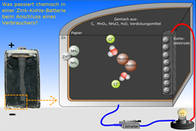
Aufbau und Funktion einer Zink-Kohle-Batterie
Eine animierte Folie auf der Webseite „chemie interaktiv“ (siehe Chemiethemen > Flash-Folien) veranschaulicht den chemischen Ablauf in einer Zink-Kohle-Batterie bei der Stromentnahme in vier Schritten. Was passiert in einer Zink-Kohle-Zelle nach Anschluss eines Verbrauchers (Glühlämpchen)?
Das Innere kann an einer aufgesägten Batterie gezeigt werden. Sie besteht aus einem Zinkbecher (als Kathode, Minus-Pol, Abgabe von Elektronen), der von einem dünnen mit einem Gemisch aus Kohlenstoff, Salmiak (=Ammoniumchlorid NH4Cl), Braunstein (=Mangandioxid MnO2) und Wasser (H2O) gefüllt ist. Im Kern befindet sich ein Kohle-Stab (als Anode, Plus-Pol, nimmt die Elektronen auf).
Bei der Entladung wird an der Kathode, dem Zinkbecher, metallisches Zink (Zn) oxidiert. Der Elektronenfluss entsteht durch diese Oxidation von Zinkatomen des Zinkbechers, bei der Elektronen frei werden. Das Mangandioxid wird dagegen reduziert, d.h. ein Elektron wird aufgenommen. Dabei entsteht Manganoxidhydroxid. Die Ammonium-Ionen geben jeweils ein Proton an OH¯-Ionen ab. Ammoniak lagert sich an die entstandenen Zink-Ionen an und bildet positiv geladene Zink-Aminkomplexe.
Ein Info-Blatterläutert den gesamten animierten Vorgang für den Lehrer.